Subscribe to RSS
DOI: 10.1055/s-0033-1344716
Frankfurter Dermatologentagung
6. November 2013, Klinik für Dermatologie, Venerologie und Allergologie, Universitätsklinikum, Goethe-Universität, Frankfurt am MainAnnual Frankfurt Dermatology MeetingNovember 6, 2013, Department of Dermatology, Venerology and Allergology, University Hospital, Goethe-University Frankfurt, MainAuthors
Xanthoma disseminatum
J. Kleemann
Anamnese: Die Vorstellung des 2-jährigen, aus Syrien stammenden Jungen erfolgte in unserer Hochschulambulanz wegen seit dem 4. Lebensmonat bestehenden gelb-bräunlichen Papeln. Diese begannen im Gesicht und breiteten sich im Verlauf auf Thorax und Extremitäten aus.
Untersuchungsbefund: Der 2-jährige Junge war ansonsten gesund. Im Gesicht, v. a. an den Wangen und den Augen, sowie am Stamm und vereinzelt den Extremitäten fanden sich zahlreiche hyperpigmentierte, gelb-braune asymptomatische Papeln, die teilweise konfluierten ([Abb. 1 a]). Außerdem zeigten sich 3 Cafe-au-lait-Flecken am Abdomen. Die Schleimhäute waren unauffällig.






Dermatohistologischer Befund: Man sah ein akanthotisches Epithel mit verlängerten Reteleisten und basaler Hyperpigmentierung. In der oberen Dermis, teils intraepidermal, fanden sich dichte Infiltrate aus kleinen und mittelgroßen monomorphen Zellen mit wabigem Zytoplasma (CD1a, [Abb. 1 b]). Immunhistochemisch waren in der Epidermis die Langerhanszellen und Langerin-positive Zellen, teils herdförmig, vermehrt, in der Dermis waren nur einzelne Zellen CD1a- bzw. Langerin-positiv. Die dermalen Infiltrate waren CD68-positiv und S100-negativ ([Abb. 1 c]). Die Proliferationsrate der Zellen war sehr gering.
Therapie und Verlauf: Klinisch und histologisch wurde die Diagnose eines Xanthoma disseminatum gestellt. Eine systemische Beteiligung konnte ausgeschlossen werden (u. a. unauffällig: augenärztlicher Befund, Röntgen-Thorax, cMRT, Sono-Abdomen, Echokardiografie), laborchemisch bestand lediglich eine hypochrome Anämie, kein Diabetes insipidus. Eine kausale Behandlung gibt es nicht, Spontanremissionen sind möglich. Derzeit erfolgen jährliche dermatologische Kontrollen.
Kommentar: Bei Xanthoma disseminatum handelt es sich um eine seltene, nichtlipämische Systemerkrankung aus dem Formenkreis der Non-Langerhans-Zellhistiozytosen (ca. 100 Fallberichte). Männer sind 2 – 3-mal häufiger betroffen als Frauen. Die Krankheit kann in jedem Alter beginnen, 50 % der Patienten erkranken vor dem 25. Lebensjahr, häufig bereits im Kindesalter (ca. 38 %). Eine familiäre oder geografische Häufung fand sich nicht. Typisch sind die teilweise konfluierenden braun-gelben bis rötlichen Papeln, Knoten und Plaques im Gesicht (v. a. Lider), an Extremitätenbeugeseiten und den Intertrigines. Der Befund entsteht durch Lipid-Ablagerungen sekundär nach Proliferation sog. histiozytärer Zellen.
Histologisch typisch ist eine diffuse dermale Infiltration durch Makrophagen und Touton-Riesenzellen, Plasmazellen und Neuotrophile. Immunhistochemisch typisch ist ein Nachweis von CD68-positiven und S100- und CD1a-negativen Infiltraten in der Dermis.
Die Erkrankung kann einerseits nur die Haut (mit und ohne Spontanremission nach Jahren) oder auch innere Organe befallen (progressive Form). Dann entstehen die Xanthome aus histiozytären, lipidhaltigen Schaumzellen auch an der Schleimhaut, den Meningen und anderen Organen. Bei Befall der Meningen der Hypophyse entsteht häufig ein Diabetes insipidus. Ein Schleimhautbefall des oberen Respirationstrakts führt zu Atemwegsobstruktionen.
Eine kurative Therapie für Xanthoma disseminatum ist bisher nicht bekannt. Eine spontane Remission ist möglich. Initial und im Verlauf sind klinische Kontrollen zum Ausschluss einer systemischen Beteiligung, vor allem eines Diabetes insipidus, erforderlich. Störende Xanthome können exzidiert, mit CO2-Laser oder flüssigem Stickstoff abgetragen werden. Bei schweren Manifestationen wurde in Einzelfällen über gute Therapieeffekte mit Cyclophosphamid bzw. kürzlich Cladribin (2-Chlorodeoxyadenosin) berichtet.
Literatur
1 Carpo B, Grevelink S, Brady S, Gellis S, Grevelink J. Treatment of Cutaneous Lesions of Xanthoma Disseminatum with a CO2 Laser. Dermatol Surg 1999; 25: 751 – 754
2 Alexander A, Turner R. Xanthoma disseminatum: a case report and literature review. Br J Radiol 2005;78: 153 – 157
3 Khezri F, Gibson LE, Tefferi A. Xanthoma disseminatum: effective therapy with 2-chlorodeoxyadenosine in a case series. Arch dermatol. 2011;147: 459 – 464
4 Seaton ED, Pillai GJ, Chu AC. Treatment of xanthoma disseminatum with cyclophosphamide. Br J Dermatol 2004;150: 346 – 349
Hyponychia congenita
W. Hofmann
Anamnese: Ein 14-jähriger Patient berichtete über seit der Geburt bestehende asymptomatische Nagelveränderungen an Händen und Füßen. Seine Geschwister, Eltern und Großeltern wiesen keine Nagelveränderungen auf. Vorerkrankungen, Zahn- oder Knochenanomalien bestanden nicht.
Untersuchungsbefund: An allen Nägeln findet sich eine Verkürzung der Nagelplatte ohne periunguale Auffälligkeiten ([Abb. 2 a u. b]). Alle Fingernägel zeigen nach lateral eine aufgeworfene, nach distal eine abgeflachte Nagelplatte, an den Zehennägeln fehlen Dystrophiezeichen. Haar-, Zahn- und Knochenstatus sind unauffällig.
Therapie und Verlauf: Nach konsiliarischer Beurteilung (Fr. Dr. Stieler, Dermatologie, Charité, Berlin) konnte die Diagnose einer Hyponychia congenita gestellt werden.
Kommentar: Bei der Hyponychia congenita handelt es sich um eine Hypoplasie der Finger- und/oder Fußnägel. Analog zu vielen Nagelerkrankungen ist auch diese eine Blickdiagnose. Kongenitale Hyponychien und Anonychien sind seltene Malformationen, welche isoliert oder als Bestandteil verschiedener Syndrome z. B. eines Nagel-Patella- oder eines Coffin-Siris-Syndroms auftreten. Im Rahmen von syndromalen Erkrankungen treten zusätzlich Anomalien anderer ektodermaler Gewebe (Alopezie, Skelett- oder Zahnanomalien, Hyper- oder Anhidrose) auf. Diese lagen bei unserem Patienten nicht vor, sodass es sich um eine isolierte, nicht-syndromale Hyponychie handelt. Bei den isolierten, nicht-syndromalen, autosomal-rezessiven kongenitalen Hypo- oder Anonychien wird der Verlust oder die Hypoplasie des Nagelmaterials durch eine Mutation im R-spondin 4-(RSPO4)-Gen hervorgerufen. Wegen mangelnder therapeutischer Konsequenz wurde bei unserem Patienten auf eine molekulargenetische Untersuchung verzichtet.


Literatur
1 Seitz CS, Hamm H. Congenital brachydactyly and nail hypoplasia: clue to bone-dependent nail formation. Br J Dermatol 2005; 152: 1339 – 1342
2 Khan TN, Klar J, Nawaz S, Jameel M, Tariq M, Malik NA, Baig SM, Dahl N. Novel missense mutation in the RSPO4 gene in congenital hyponychia and evidence for a polymorphic initiation codon (p.M1 l). BMC Medical Genetics 2012; 13: 120
Psoriatische Nageldystrophie
A. Barudoni
Anamnese: Bei der mittlerweile 22-jährigen Patientin bestehen seit dem 1. Lebensjahr Hautveränderungen an den Fingerkuppen und Nagelveränderungen im Sinne einer Onychodystrophie. Eine Tinea wurde ausgeschlossen. Im Laufe der Jahre breiteten sich die Hautveränderungen auf die Füße, seit 2 Jahren auf das Capillitium und die Schienbeine aus. Die Patientin gibt keine Schmerzen an, die Endgelenke seien immer wieder angeschwollen.
Die Vortherapie erfolgte von 2005 bis 2007 erfolglos mit Acitretin, lokal mit Steroiden, Calcipotriol und Tacrolimus. Eine systemische Therapie mit Ciclosporin A über 3 Monate zeigte keine Wirkung.
Untersuchungsbefund: Man sah an allen Nägeln (20/20) eine Onychodystrophie mit subungualen Hyperkeratosen ([Abb. 3 a]). An den Fingerkuppen fanden sich Schuppung und Rhagaden und am rechten Schienbein ein randbetonter, erythematöser, leicht squamöser Plaque ([Abb. 3 b]).




Diagnostik: Die Probebiopsie am rechten Schienbein zeigte eine kompakte Parakeratose über einem
fokal schwach ausgeprägten Stratum granulosum. Die Epidermis war akanthotisch verbreitert
bei hochreichenden, vaskularisierten Papillenspitzen. Im oberen Bindegewebe erkannte
man ein moderates, vorwiegend lymphozytäres Entzündungsinfiltrat. In der Alcian-PAS-Färbung
waren keine Pilzelemente nachweisbar.
Das Röntgenbild von Händen und Füßen zeigt keine Arthritis. In der Arthrosonographie
fand sich ein deutliches Powerdopplersignal an der Nagelmatrix, aber keine floride
Arthritis.
Therapie und Verlauf: Unter der Diagnose einer Psoriasis mit erhöhtem Risiko für die Entwicklung einer Psoriasis-Arthritis leiteten wir, nach Ausschluss von Kontraindikationen, eine Therapie mit Methotrexat s. c. in einer Dosis von 10 mg/Woche ein. Im weiteren Verlauf wurde die Dosis bei guter Verträglichkeit auf 15 mg/Woche erhöht. Zwei Tage nach der Injektion von Methotrexat wurde Folsäure 5 mg eingenommen.
Kommentar: Die Nagelpsoriasis ist eine häufige und besonders bei schwerer Ausprägung für den Patienten stark belastende Manifestation der Psoriasis. Etwa die Hälfte der Patienten mit Psoriasis leidet an einer Beteiligung der Nägel. Die Nagelpsoriasis kann aber auch bei 1 – 5 % der Fälle ohne weitere Erscheinungsformen auftreten. Bei Patienten mit Psoriasis-Arthritis (PsA) liegt die Prävalenz bei ca. 70 % im Vergleich zu ca. 40 % bei Patienten ohne PsA. Die Ursache dafür ist wahrscheinlich der anatomische Kontakt zwischen Nagelapparat und distalem Interphalangealgelenk. Bei mehr als der Hälfte der Betroffenen führt die Nagelpsoriasis zu Schmerzen, funktioneller Einschränkung und psychischer Belastung mit negativer Auswirkung auf das Berufs- und Sozialleben. Deshalb, aber auch als mögliches frühes Zeichen einer PsA sollte die Nagelpsoriasis ernst genommen werden.
Es gibt nur wenig Evidenz zur Wirksamkeit lokaler Therapieformen. Trotz nur leicht ausgeprägter Hautveränderungen ist bei schwerer Nagelpsoriasis eine systemische Therapie indiziert. Für die Biologica und für Methotrexat liegen solide Studiendaten vor, die zeigen, dass bei kontinuierlicher Therapie über mehrere Monate eine deutliche Verbesserung erreicht werden kann.
Literatur
1 Yasemin O, Deniz A. Treatment of nail psoriasis: common concepts and new trends. Dermatol Res Pract, 2013; Volume 2013; ID 180496
2 Lawry M. Biological therapy and nail psoriasis. Dermatol Ther 2007; 20: 60 – 67
3 Kahl C, Hansen B, Reich K. „Stiefkind“ Nagelpsoriasis. Hautarzt 2012; 63: 184 – 191
4 Gümüsel M, Özdemir M, Mevlitoglu I, Bodur S. Evaluation of the efficacy of metothrexate and cyclosporine therapies on psoriatic nails: a one-blind, randomized study. J Eur Acad Dermatol Venereol. 2007: 25: 1080 – 1084
5 de Vries AC, Bogaards NA, Hooft L, Velema M, Pasch M, Lebwohl M, Spuls PI. Interventions for nail psoriasis. Cochrane Database Syst Rev 2013 CD007633; doi: 10.1002/14651858
Naevoides Teleangiektasiesyndrom
C.-F. Pfeiffer
Anamnese: Der 23-jährige Patient berichtet über seit ca. 10 Jahren langsam zunehmende Rötungen im Gesicht, am oberen Stamm und an den Armen. Vortherapien mit Isotretinoin für zweimal sechs Monate und Lokaltherapien mit diversen Aknetherapeutika seien bislang erfolglos geblieben. Es bestehen keine Vorerkrankungen, es werden keine Medikamente, gelegentlich Alkohol konsumiert. Der Vater leidet an Rosazea, der Bruder an Akne.
Körperlicher Untersuchungsbefund: 23-jähriger Patient, wach und voll orientiert, in gutem AZ und schlankem EZ.
Dermatologischer Untersuchungsbefund: Es fanden sich betont zentrofazial, distal über Hals und Schulter sowie auf der linken Seite über Ober- und Unterarm bis zum Handrücken reichend, multiple, dicht stehende Teleangiektasien.
Therapie und Verlauf: Es wurde eine Lasertherapie (Diodenlaser bzw. IPL) geplant.
Kommentar: Das naevoide Teleangiektasie-Syndrom ist ein seltenes Krankheitsbild. Erstmals beschrieben wurde es von Alfred Blaschko im Jahre 1899. Charakteristisch sind bevorzugt unilateral und dermatombezogen auftretende Teleangiektasien. Insbesondere das Versorgungsgebiet des Nervus trigeminus sowie die zervikalen und oberen thorakalen Dermatome sind betroffen. Die Teleangiektasien können so dicht zusammentreten , dass sie wie eine homogene Rötung wirken, das teleangiektatische Erythem.
Die Erkrankung betrifft häufiger Frauen (m : w = 1 : 2). Sie kann angeboren sein oder erst später im Leben auftreten. Diese erworbenen Formen überwiegen. Die initiale Manifestation ist häufig mit hyperöstrogenen Zuständen assoziiert. Dies erklärt ein gehäuftes Auftreten in der Schwangerschaft, der Pubertät und bei Hepatopathien. Die Verteilung spricht für eine nävoide Fehlbildung.
Histologisch finden sich bevorzugt in der Dermis Gefäßektasien, ohne Zeichen einer endothelialen Zellproliferation und ohne Zunahme von Östrogen- bzw. Progesteronrezeptoren. Therapeutisch symptomatisch können Gefäßlaser, wie gepulster Farbstofflaser, Diodenlaser oder Blitzlampen eingesetzt werden.
Literatur
1 Wenson SF, Jan F, Sepehr A. Unilateral nevoid telangiectasia syndrome: a case report and review of the literature. Dermatol Online J 2011; 15; 17 (5): 2
2 Kreft B, Marsch WC, Wohlrab J. Unilateral Nevoid Telangiectasia Syndrome. Dermatology 2004; 209: 215 – 217
Melkersson-Rosenthal-Syndrom der Augenlider
A. Clouth
Anamnese: Bei der 52-jährigen Patientin schwollen seit 6 Monaten rezidivierend das linke Augenlid, später auch das rechte Augenlid an. Es bestand Juckreiz. Unter der klinischen Verdachtsdiagnose einer Dakryoadenitis wurde sie in der Augenklinik topisch sowie systemisch antibiotisch behandelt. Darunter besserte sich der Befund nur leicht.
Untersuchungsbefund: Bei Erstvorstellung waren beide Oberlider livide verfärbt und geschwollen ([Abb. 4 a]). Es fand sich eine konjunktivale Injektion, keine Fazialisparese.


Diagnostik: Ein CT der NNH mit KM zeigte eine Weichteilschwellung (DD: Lidphlegmone).
Die ophthalmologische Vorstellung ergab keine pathologischen Befunde. Im Abstrich
war Pseudomonas aeruginosa nachweisbar. CK, TSH, ANA sowie ANCA waren unauffällig.
Feingeweblich fand sich in der Dermis ein mäßig dichtes, teils granulomatöses Infiltrat
aus Lymphozyten, Makrophagen und einigen Neutrophilen ([Abb. 4 c]).
Diagnose: Granulomatöse Entzündungsreaktion im Sinne eines isolierten Melkersson-Rosenthal-Syndroms.
Therapie und Verlauf: Unter einer systemischen Behandlung mit Methylprednisolon verschwand die Schwellung; rezidivierte jedoch nach Absetzen. Deshalb wurde eine Therapie mit Fumarsäureestern in aufsteigender Dosierung, initial überlappend mit systemischen Steroiden, eingeleitet. Hierunter war der Befund rückläufig ([Abb. 4 b]).
Kommentar: Die klassische Trias des Melkersson-Rosenthal-Syndroms (MRS) bestehend aus Lingua plicata, rezidivierender orofazialer Schwellung sowie Fazialisparese findet sich nicht in allen Fällen in kompletter Ausprägung. Über ein isoliertes Auftreten eines MRS der Augenlider wurde berichtet. Histologisch sieht man eine granulomatöse sowie perivaskuläre Entzündung mit dermalem Ödem. Die Behandlung ist schwierig. In der Literatur genannte Optionen sind die systemische sowie intraläsionale Anwendung von Steroiden, diverse Antibiotika, Immunmodulatoren sowie Fumarsäureester. Die letztgenannte Therapie war im vorgestellten Fall erfolgreich.
Literatur
1 Rawlings NG, Valenzuela AA, Allen LH, Heathcote JG. Isolated eyelid edema in Melkersson-Rosenthal syndrome: a case series. Eye 2012; 26: 163 – 166
2 Banks T, Gada S. A comprehensive review of current treatments for granulomatous cheilitis. Br J Dermatol 2011; 166: 934 – 937
Apokrine Miliaria (Morbus Fox-Fordyce)
G. Hubatsch
Anamnese: Die Patientin hat seit ca. 10 Jahren konstant bestehend Hautveränderungen in beiden Axillen (rechts mehr als links). Die weitere Anamnese ist unauffällig. Es besteht gelegentlich Juckreiz mit Symptomverschlechterung im Sommer. Keine Medikamente, keine Allergien, keine Grunderkrankungen.
Körperlicher Untersuchungsbefund: Die 30-jährige Patientin, Hauttyp 5, ist in gutem AZ und schlankem EZ.
Dermatologischer Untersuchungsbefund: Es finden sich gruppiert stehende, stecknadelkopfgroße, plane oder halbkugelige, derbe, hyperpigmentierte Knötchen ([Abb. 5]). Es besteht leichter lokalisierter Juckreiz, keine Schweißausbrüche.


Dermatohistologischer Befund: Es zeigte sich ein standorttypisches Oberflächenepithel, Hornpfröpfe im Bereich der Schweißdrüsenausführungsgänge sowie oberflächlich dermal eine perivaskuläre lymphozytäre Entzündungsreaktion .
Therapie und Verlauf: Es wurde eine topische Schälbehandlung mit Retinoiden (Tretinoin 0,05 %-Creme) zur Nacht eingeleitet. Darunter besserte sich der Befund langsam.
Kommentar: Bei den apokrinen Miliaria handelt es sich um einen seltenen, zu Juckreiz und Papelbildung führenden Verschluss der Ausführungsgänge apokriner Schweißdrüsen. Ein hyperkeratotischer Pfropf im obersten Anteil des Haarfollikels führt zur Dilatation der Drüsenendstücke, welche sich mit PAS-positivem Material füllen; umgebend findet sich dann oft entzündliches Infiltrat. Prädilektionsstellen sind Achseln, Mamillen und Genitalregion. Klinisch sieht man gleichmäßig verteilte, weiche, zur Tiefe derbe, follikelgebundene, hautfarbene bis rötlich-braune Papeln.
Die Ätiologie ist unklar. Es scheint einen Zusammenhang mit einer hormonellen Stimulation zu geben, denn die Erkrankung betrifft v. a. Frauen nach der Pubertät mit Befundbesserung nach der Menopause. Behandlungsresultate sind oft unbefriedigend, eine Standardtherapie existiert nicht. Empfohlen werden als oberflächliche Schälbehandlung Vitamin-A-Säure-haltige Externa, neuere Ansätze sehen eine Entzündungshemmung als kausalen Therapieansatz. Hier zeigt Pimecrolimus bei sehr gutem Nutzen-Risikoprofil gute Einzelfallergebnisse. Glukokortikosteroide sind durch eine mögliche Hautatrophie nicht indiziert.
Bei schwerer Ausprägung und ausbleibendem Erfolg einer reinen Lokaltherapie können Kontrazeptiva mit antiandrogener Wirkung oder Isotretinoin p. o. verabreicht werden. Eine definitive Heilung kann letztlich nur durch eine chirurgische Intervention erzielt werden.
Literatur
1 Milcic D, Nikolic M. Clinical effects of topical pimecrolimus in a patient with Fox-Fordyce disease. Australas J Dermatol 2012; 53: e34 – 35
2 Pock L, Svrcková M, Machácková R, Hercogová J. Pimecrolimus is effective in Fox-Fordyce disease. Int J Dermatol 2006; 45: 1134 – 1135
Aggressives, diffus großzelliges B-Zell-Lymphom bei einem Kind
W. Hofmann
Anamnese: Eine 13-jährige Patientin berichtete über plötzlich aufgetretene, seit 3 Monaten bestehende, symptomlose Schwellungen des Halses und Dekolletés bei sonst gutem Allgemeinzustand. Zahlreiche antibiotische Vortherapien waren erfolglos. ?>Unter wiederholter Applikation systemischer Steroide (p. o., i. m., intraläsional) bildeten sich die Hautveränderungen zurück, rezidivierten aber rasch nach Absetzen. Bis auf die üblichen Infektionen des Kindesalters war die Anamnese unauffällig.
Untersuchungsbefund: Klinisch präsentierten sich zervikal beidseits, rechts bis zur Klavikula reichende, scharf begrenzte, gelblich-rote, kissenartig aufgeworfene, mehrere cm große, verhärtete und überwärmte Plaques ([Abb. 6 a]). Die zervikalen Lymphknoten waren vergrößert. Die Halsbeugung nach links und nach vorne war eingeschränkt.


Histologisch zeigte sich unter einer unauffälligen Epidermis in der tieferen Dermis und dem Subkutangewebe bis zu den zur Darstellung kommenden Muskelstrukturen ein dichtes, CD20-positives Blasteninfiltrat ([Abb. 6 b – d]). Proliferationsrate (Ki67) über 90 %. Die Klonalitätsanalyse bestätigte ein monoklonales Muster mit Nachweis eines diffus großzelligen B-Zell-Lymphoms. Im PET-CT zeigte sich neben den äußerlich sichtbaren Herden auch der hochgradige Verdacht auf eine Mitbeteiligung der dorsalen Schultergürtel- und Thoraxwandmuskulatur, des M. erector spinae und M. psoas rechts, des Zwerchfellschenkels rechts medial, des Marklagers des linken Schambeinastes und der Tonsillenlogen. Eine Knochenmarkstanze, die Lumbalpunktion und ein cMRT waren ohne Pathologien.
Therapie und Verlauf: Es erfolgte eine Polychemotherapie nach NHL-BFM Registry 2012 ohne konsolidierende Radiatio (Kinderklinik der Uniklinik Frankfurt, Prof. Dr. Klingebiel). Bereits nach Abschluss des 1. Therapiezyklus konnte die Patientin ihren Hals wieder nahezu normal bewegen. Im PET-CT zeigte sich nur noch eine geringe Restaktivität. Komplizierend traten unter Immunsuppression eine Mukositis, eine Pneumonie sowie eine Pilzinfektion auf, sodass längere Krankenhausaufenthalte erforderlich waren. Aktuell befindet sich die Patientin kurz vor Beendigung der Chemotherapie in gutem Allgemeinzustand und nahezu kompletter Remission.
Kommentar: Unser Fallbericht präsentiert eine eindrucksvolle, sehr seltene klinische Manifestation eines B-Zell-Non-Hodgkin-Lymphoms bei einem Kind. Diffus großzellige B-Zell-Lymphome machen nur ca. 10 % der Non-Hodgkin-Lymphome (NHL) des Kindes- und Jugendalters aus. Im Unterschied zu den NHL des Erwachsenenalters zeichnen sich diese im Kindes- und Jugendalter durch ein sehr aggressives Wachstum aus. Bis in die 70er-Jahre war die Überlebensprognose von Kindern mit NHL fast infaust. Nach großen kooperativen multizentrischen Therapiestudien (z. B. der Berlin-Frankfurt-Münster-Gruppe = BFM), nach deren Protokollen je nach Subgruppe des NHL die Therapie bis heute erfolgt, können heutzutage hohe Überlebensraten erzielt werden. Im Zentrum dieser Behandlungen stehen Polychemotherapien, welche lokale Therapiemaßnahmen inkl. Strahlentherapien weitestgehend ersetzt haben.
Literatur
1 Reiter A. Non-Hodgkin Lymphoma in Children and Adolescents. Klin Padiatr 2013; 225: 87 – 93
2 Lange J, Burkhardt B. Treatment of Adolescents with Aggressive B-Cell Malignancies: The Pediatric Expierence. Curr Hematol Malig Rep 2013 (ahead of print; PMID: 23812872)
3 Meyer-Wentrup F, de Zwart V, Bierings M. Antibody therapy of pediatric B-cell lymphoma. Frontiers in Oncology 2013; 3: 1 – 8
Angiosarkom – zwei Fallbeispiele einer seltenen Diagnose
K. Schultheis
Anamnese: Patientin 1: Eine 79-jährige Patientin stellte sich mit einem seit ca. einem halben Jahr bestehenden, nicht schmerzhaften Knoten der Kopfhaut vor. Es waren bereits mehrfache Konsultationen bei verschiedenen Ärzten aufgrund rezidivierender Blutungen vorausgegangen.
Patientin 2: Eine 73-jährige Patientin hatte seit ca. drei Monaten das Wachstum eines Knotens an der Kopfhaut bemerkt. Histologisch konnte ein Angiosarkom gesichert werden.
Untersuchungsbefund: Patientin 1: Parietal fand sich ein ca. 2 × 3 cm großer, livider und blutender Knoten ([Abb. 7 a]). Histologisch wurde ein Angiosarkom gesichert ([Abb. 7 c, d]).
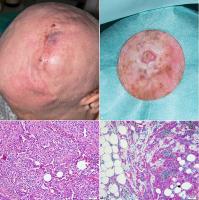

Patientin 2: Parieto-frontal sah man eine bläulich livide, unscharf begrenzte, ca. 3 × 2 cm große Makula mit vereinzelten Ulzera ([Abb. 7 b]).
Diagnostik: Bei Patientin 1 erfolgte die mikrografisch kontrollierte Exzision des bei Aufnahme noch unbekannten Tumors. Histologisch zeigte sich ein Angiosarkom.
Bei beiden Patienten erfolgte ein Staging mittels CT Thorax/Abdomen, MRT Schädel und eine LK-Sonografie. Bei Patientin 1 ergab sich kein Anhalt für eine Fernmetastasierung.
Patientin 2 zeigte bereits Metastasen.
Therapie und Verlauf: Bei Patientin 1 konnte der Tumor in sano (R0) reseziert werden. Der Defekt wurde mittels VAC-Anlage, Integraeinlage und Spalthaut gedeckt. Eine postoperative Radiatio war geplant. Am geplanten Entlassungstag klagte die Patientin über starke Dyspnoe. Bei erhöhten D-Dimer-Werten wurde bei Verdacht auf eine Lungenembolie ein CT durchgeführt. Hier zeigte sich eine fulminante, innerhalb von 2 Monaten neu aufgetretene Lungenmetastasierung mit zusätzlich vorhandenem Pleuraerguss. Die Patientin lehnte jedoch jegliche weitere Intervention ab, sodass sie einige Tage später bei uns verstarb.
Bei Patientin 2 konnte aufgrund der Größe des Befundes nur eine Resektion mit Residualtumor (R1) erfolgen. Wegen des bereits fortgeschrittenen Stadiums mit Metastasierung entschieden wir uns für eine metronome Chemotherapie mit antiangiogener Zielrichtung bestehend aus einer Dreifachkombination aus Pioglitazon, Rofecoxib und Trofosfamid. Hierunter zeigte sich 6 Monate lang eine stable disease. Die Therapie wurde gut vertragen. Leider entwickelte sich dann ein weiterer Progress der Erkrankung mit einer fulminanten Lungenmetastasierung, woran die Patientin dann verstarb.
Kommentar: Das Angiosarkom ist ein seltener hochmaligner Tumor, der von den Endothelzellen von Blut- und Lymphgefäßen ausgeht [1].
Klinisch zeigen sich unterschiedliche Bilder. Initial sieht man meist unscharfe rote Makulae mit Teleangiektasien, welche im Verlauf wachsen, später Knoten bilden und sich livide verfärben. Häufig wird von rezidivierenden Blutungen berichtet. Typisch ist das diskontinuierliche Wachstum des Tumors mit Ausbildung von tumorfreien Arealen. Eine komplette Entfernung des Tumors ist daher oft schwer möglich. Histologisch zeigen sich oberflächliche Teleangiektasien mit endothelialen Atypien, vakuolisierte Tumorzellen, sowie mehrschichtige intravasale Endothelknospen. Die immunhistologischen Antikörper CD31, CD34 helfen bei der Diagnosestellung.
Die Prognose ist schlecht mit meist foudroyanten Verläufen. Die 5-JÜR liegt bei < 10 %. Die Metastasierung erfolgt meist hämatogen in die Lunge oder lymphogen in regionäre LK.
Wichtigste Therapiesäule ist die chirurgische Entfernung der Läsion. Nach einer R0-Resektion sollte eine postoperative Radiatio erfolgen. Im bereits metastasierten Stadium kommen palliative systemische Therapien zur Anwendung. Ein einheitliches Therapieschema gibt es nicht [2]. Neben systemischen Chemotherapien ist die ambulante Therapie mit einer Kombination mit Trofosfamid, Coxiben, und Pioglitazon eine Alternative mit geringer Toxizität [3].
Da die Diagnose sehr selten ist, gibt es nur wenige Studien mit großen Fallzahlen.
Literatur
1 Penel N, Marreaud S, Robin YM, Hohenberger P. Angiosarcoma: state of the art and perspectives. Crit Rev Oncol Hematol 2011; 80: 257 – 263
2 Vogt T, Brockmeyer N, Kutzner H, Schöfer H. Short German guidelines: angiosarcoma and Kaposi sarcoma. J Dtsch Dermatol Ges 2008; 6 (Suppl. 1): S19 – 24
3 Vogt T, Hafner C, Bross K, Bataille F, Jauch KW, Berand A, Landthaler M, Andreesen R, Reichle A. Antiangiogenetic therapy with pioglitazone, rofecoxib, and metronomic trofosfamide in patients with advanced malignant vascular tumors. Cancer 2003; 98: 2251 – 2256
Basalzellkarzinome – Neue Therapie mit small molecules
A. Pinter
Anamnese: Der 70-jährige Patient ist seit Ende 2007 wegen eines gesicherten Gorlin-Goltz-Syndroms in unserer regelmäßigen ambulanten und stationären Behandlung. Durch langjährige Aufenthalte in Äquatornähe hatte der Patient durch den UV-Einfluss seine genetisch determinierte Neigung zu Basalzellkarzinomen zusätzlich verstärkt. Neben multiplen, teilweise mutilierenden chirurgischen Eingriffen wurden auch Retinoide und photodynamische Therapien durchgeführt, um das Fortschreiten zu verhindern.
Befund: Am gesamten Integument mit Betonung des Gesichtes, des Nackens und der Schulterregion sowie der distalen Extremitätenanteile zeigten sich multiple, teilweise konfluierende, flache, vereinzelt ulzerierende Basalzellkarzinome ([Abb. 8 a]). Hinweise auf weitere nichtmelanozytäre Malignome oder Melanome gab es nicht. Weitere Hauterkrankungen waren nicht bekannt.


Therapie: Im Rahmen einer klinischen Studie erhielt der Patient über einen Zeitraum von 60 Wochen einmal täglich 150 mg Vismodegib p. o. Innerhalb von 24 Wochen bildeten sich alle Basalzellkarzinome des Patienten zurück, sodass klinisch keine Tumore mehr zu erkennen waren. Dieser Zustand blieb über einen Zeitraum von weiteren 24 Wochen stabil ([Abb. 8 b]). Die Therapie musste aufgrund von Muskelkrämpfen und Geschmacksstörungen mehrfach für wenige Wochen pausiert werden. Nach einem Jahr unter der Therapie mit Vismodegib wuchs erstmalig, histologisch gesichert, erneut ein einzelnes Basalzellkarzinom. Die Lebensqualität war unter den Nebenwirkungen zwar eingeschränkt, trotzdem war der Patient mit der Behandlung sehr zufrieden.
Kommentar: Die Therapie multipler, inoperabel fortgeschrittener oder metastasierter Basalzellkarzinome stellt Therapeuten oft vor große Herausforderungen. Neben der operativen Exzision kann, bis auf Patienten mit Gorlin-Goltz-Syndrom, auch eine Radiotherapie eingesetzt werden. Lokale Therapeutika wie Immunmodulatoren (Imiquimod) bzw. Zytostatika (5-Fluorouracil) können bei geringer Tumorlast Off-label gegeben werden. Eine neue Therapieoption bei fortgeschrittenen, inoperablen Basalzellkarzinomen steht mit dem im Juli 2013 zugelassenen Smoothened-Rezeptor-Antagonisten Vismodegib zur Verfügung. Das einmal täglich oral einzunehmende Medikament entfaltet seine Wirkung durch die Inaktivierung des konstitutiv aktiven Proteins Smoothened. Dies führt zu einer Transkriptionshemmung von Genen, die am Tumorwachstum beteiligt sind. Häufige, aber stets reversible Nebenwirkungen sind neben Geschmacksstörung und dadurch bedingtem Gewichtsverlust auch Muskelkrämpfe und Haarausfall. Mit der Zulassung von Vismodegib wird die Therapieoption bei Basalzellkarzinomen potent erweitert. Die Behandlung sollte aber ausschließlich bei inoperablen, metastasierten Tumoren oder bei Patienten mit Gorlin-Goltz-Syndrom verwendet werden.
Literatur
1 Sekulic A, Migden MR, Oro AE, Dirix L, Lewis KD, Hainsworth JD, Solomon JA, Yoo S, Arron ST. Efficacy and safety of vismodegib in advanced basal-cell carcinoma. N Engl J Med 2012; 366: 2171 – 2179
2 Henkin RI. Vismodegib in advanced basal-cell carcinoma. N Engl J Med 2012: 367: 970
3 Sekulic A, Migden MR, Oro AE, Dirix L, Lewis KD, Hainsworth JD, Solomon JA, Yoo S, Arron ST. Surgical excision after neoadjuvant therapy with vismodegib for a locally advanced basal cell carcinoma and resistant basal carcinomas in Gorlin syndrome. JAMA Dermatol 2013; 149: 639 – 641
Eine paradoxe Reaktion unter Biologikatherapie bei Psoriasis vulgaris
B. Malisiewicz
Anamnese: Der 53-jährige Patient leidet seit 1995 an einer Psoriasis vulgaris und Psoriasis pustulosa ohne Gelenkbeteiligung. Er wurde mit diversen Externa und Systemtherapeutika mit unzureichendem Erfolg behandelt. Seit Juni 2012 erhielt der Patient daher Ustekinumab in einer Dosis von 90 mg. Hierunter besserte sich die Psoriasis deutlich. 8 Wochen nach Therapiebeginn traten an den oberen Extremitäten und teils am Rumpf neue juckende Hautveränderungen auf.
Untersuchungsbefund: Es fanden sich, neben typischen psoriatischen Hautveränderungen, streckseitig an beiden Unterarmen sowie vereinzelt am Stamm nässende, teils exkoriierte, teils krustös belegte Plaques.
?>Diagnostik: Abstriche ergaben eine reichliche Besiedelung mit Staphylococcus aureus. Das Gesamt-IgE war normwertig (13 IU/ml [0,1 – 87 IU/ml]). Histologisch zeigte sich ein Mischbild aus einer Psoriasis und einem Ekzem.
Therapie und Verlauf: In Zusammenschau der Klinik und Histologie wurde die Diagnose einer sogenannten paradoxen Reaktion, d. h. der Entwicklung einer atopischen Dermatitis auf Ustekinumab gestellt. Es wurde additiv mit 7,5 mg initial, dann mit 15 mg Methotrexat (subkutan, 1 × wöchentlich) und zusätzlichen kortikosteroidhaltigen Externa behandelt. Hierunter besserte sich der Hautbefund deutlich. Wegen steigender Leber- und Nierenwerte musste Methotrexat abgesetzt werden. Der Befund blieb unter Fortführung der Ustekinumabtherapie und intermittierender topischer Kortikosteroide stabil.
Kommentar: Seit Markteinführung und dem breiten Einsatz von Biologika für Psoriasis wurden diverse neue Nebenwirkungen beschrieben. Neben paradoxen Reaktionen, wie dem Auftreten einer Psoriasis unter einer TNF-α-Blockade bei Morbus Crohn, wurden Erkrankungen aus dem atopischen Formenkreis beschrieben:
-
Asthma mit konsekutiver peripherer Eosinophilie unter Adalimumab
-
eine isolierte periphere Eosinophilie als Ausdruck einer verstärkten Th2-Immunantwort
-
gleichzeitiges Auftreten sowohl einer Psoriasis als auch einer atopischen Dermatitis; unter Biologika besserte sich die Psoriasis, die atopische Dermatitis verschlechterte sich dagegen.
Pathophysiologisch werden die Psoriasis und der atopische Formenkreis durch unterschiedliche T-Zell-Aktivierungsmuster charakterisiert: Während die Psoriasis Th1-/Th17-Zell-dominiert ist, weist die Atopie eine Th2-Polarisation auf. Die wechselseitige Hemmung dieser Zelltypen erklärt die oben beschriebenen Reaktionen:
Hemmt man den Th1-/Th17-Arm, überwiegt die Th2-Immunantwort und klinisch entsteht ein Ekzem.
Während für das Auftreten einer Psoriasis unter TNF-α-Inhibition schon Behandlungsalgorithmen vorliegen, fehlen diese für Reaktionen aus dem atopischen Formenkreis. Es wird in erster Linie eine additive topische Therapie mit Steroiden empfohlen oder eine systemische Therapie mit Immunsuppressiva, die sowohl bei der Psoriasis als auch bei der atopischen Dermatitis eingesetzt werden. Die Behandlung ist aber auf den Einzelfall abzustimmen.




Literatur
1 Bennett AN, Wong M, Zain A, Panayi G, Kirkham B. Adalimumab-induced Asthma. Rheumatology (Oxford) 2005; 44:1199 – 1200
2 Collamer AN, Bataffarano DF. Psoriatic skin leasions by tumor necrosis factor antagonist therapy: clinical features and possible immunopathogenesis. Semin Arthritis Rheum 2010; 40: 233 – 240
3 Malisiewicz B, Murer C, Pachlopnik-Schmid J, French LE, Schmid-Grendelmeier P, Navarini AA. Eosinophilia during Psoriasis Treatment with TNF Antagonists. Dermatology 2011; 223: 311 – 315
4 Eyerich S, Onken AT, Weidinger S, Franke A, Nasorri F, Pennino D, Grosber M, Pfab F, Schmidt-Weber CB, Mempel M, Hein R, Ring J, Cavani A, Eyerich K. Mutual Antagonism of T Cells Causing Psoriasis and Atopic Eczema. N Engl J Med 2011; 365: 231 – 238
5 Deleuran MS, Vestergaard C. Therapy of severe atopic dermatitis in adults. J Dtsch Dermatol Ges 2012; 10: 399 – 406
Steroidatrophie bei der topischen Anwendung moderner Kortikosteroide
K. Mauer
Anamnese: Die Patientin stellte sich wegen seit fünf Jahren bestehenden Rötungen und Schwellungen im Gesicht und am Dekolleté unter dem Verdacht auf eine Kollagenose vor. Erste Hautveränderungen sollen ungefähr ein halbes Jahr nach zwei Kieferoperationen unter Lokalanästhesie mit Ultracain aufgetreten sein
Im Laufe der Zeit bemerkte sie vor allem an den Armen, im Gesicht und Dekolleté eine erhöhte Verletzlichkeit und Einblutungen der Haut. Extern konnte der Verdacht auf einen Lupus erythematodes nicht bestätigt werden, die Diagnostik bezüglich eines Von-Willebrand-Syndroms blieb ohne eindeutiges Ergebnis.
Untersuchungsbefund: An Wangen und Stirn zeigten sich multiple, millimetergroße rötliche Papeln, konfluierend bis zu ca. 2 cm messenden Plaques auf einer flächigen Rötung mit kleinen Einblutungen ([Abb. 10 a]). An beiden Unterarmen und im Dekolleté war die Haut atroph, man sah Teleangiektasien, Purpura, Sugillationen und Ekchymosen ([Abb. 10 b]).




Diagnostik: Für eine Kollagenose fand sich kein Anhalt (ANAs negativ). Im Labor zeigte sich ein CRP-Wert von 4,15 mg/dl und Leukozyten initial bei 9,55/nl, dann 5,52/nl. Ein Pustelabstrich war steril. Eine intensive Befragung ergab, dass die Patientin seit Beginn der Hautveränderungen konstant einmal täglich Mometasonfuroat-Fettcreme und eine fettreiche homöopathische Salbe im Gesicht anwandte. Wir stellten die Diagnose einer perioralen Dermatitis, einer Fettreizung und Steroidatrophie. Klinisch und laborchemisch zeigte sich kein Anhalt einer Beeinträchtigung der Hypophysen-Nebennierenrinden-Achse oder Anzeichen eines Cushing-Syndroms.
Therapie und Verlauf: Es wurde mit Metronidazolcreme und Zinköl, später mit weicher Zinkpaste behandelt. Unter dieser Therapie verschlechterte sich der Befund mit starkem Erythem, Schwellung und vermehrter Pustelbildung im Gesicht. Bei unveränderter Lokaltherapie und zusätzlich Doxycyclin 50 mg (38 Tage) einmal täglich besserte sich der Befund im Gesicht, die Einblutungen in die Haut ließen nach und die Leukozyten im Blut fielen ab.
Kommentar: Momethasonfuroat hat im Vergleich mit anderen topischen Kortikosteroiden eine sehr gute Risiko-/Nutzenbewertung [1, 2]. Es erhielt, wie Prednicarbat und Methylprednisolonaceponat, den höchsten TIX-Wert (Therapeutischer Index) von 2,0. Dieser Wert wird anhand folgender Variablen errechnet: Vasokonstriktion, Wirksamkeit bei atopischer Dermatitis (AD), Hautatrophie, Wirkung auf die Hypophysen-Nebennierenrinden-Achse (HNNR), allergenes Potenzial. Bisher ging man davon aus, dass bei sachgemäßer Anwendung keine Systemeffekte zu erwarten seien. Unsere Patientin verwendete jedoch über Jahre hinweg Mometasonfuroat-Fettcreme im Gesicht. Sie entwickelte eine Steroidatrophie in anwendungsfreien Arealen (Unterarme). Dies zeigt, dass auch moderne Kortikosteroide bei unsachgemäßer Anwendung systemische Nebenwirkungen verursachen können [3]. Bei einer längerfristigen und hochdosierten, lokalen sowie systemischen Kortikosteroidapplikation (inhalativ und oral) wird Kollagen I und III reduziert. Dies ist auch ohne Beeinträchtigung der Hypophysen-NNR-Achse möglich und geht mit Verdünnung und erhöhter Verletzlichkeit der Haut einher [4]. Eine gute Aufklärung der Patienten bei Ausgabe jeglicher steroidhaltiger Externa ist nach wie vor erforderlich.
Literatur
1 Luger T, Elsner P, Kerscher M, Korting HC. Topische Dermatotherapie mit Glukokortikoiden – Therapeutischer Index. J Dtsch Dermatol Ges 2003 (Aktualisierung 01/2009); http://awmf.org/
2 Mirshahpanah P, Döcke W-D, Merbold U. Superior nuclear receptor selectivity and therapeutic index of methylprednisolone aceponate versus mometasone furoate. Exp Dermatol 2004; 16: 753 – 761
3 Lynette K, Nieman, MD. Consequences of systemic absorption of topical glucocorticoids. J Am Acad Dermatol 2011; 65: 250 – 252
4 Autio P, Karjalainen J, Risteli L, Risteli J, Kiistala U, Oikarinen A. Effects of an inhaled steroid (budesonide) on skin collagen synthesis of asthma patients in vivo. Am J Resp Crit Care Med 1996; 153: 1172 – 1175
Schuppende Erytheme nach Diclofenac 3 %-Gel
C. Schopper
Anamnese: Bei einem 64-jährigen Patienten trat 4 Wochen nach der Anwendung von Diclofenac 3 %-Gel in 2,5 Prozent Hyaluronsäure (Solaraze®-Gel, 2 ×/Tag) wegen flächenhafter aktinischer Keratosen eine juckende, teilweise nässende Rötung der Kopfhaut auf.
Zeitgleich wurde der Patient aufgrund eines Harnwegsinfektes mit Ciprofloxacin behandelt.
Unter einem Steroidstoß mit 80 mg Methylprednisolon und lokal Fucidine® heilten die Hautveränderungen schnell ab.
Die Reaktion wurde als Unverträglichkeit auf Solaraze® angesehen.
Zwei Monate später wurde Ciprofloxacin erneut eingenommen. Ein Tag nach Einnahme entwickelte sich eine starke Entzündung der Kopfhaut und im Verlauf ein Exanthem am gesamten Körper. Aufgrund dieser Symptomatik wurden nun beide Reaktionen als Unverträglichkeit auf Ciprofloxacin gewertet.
Zwei Jahre später wurden die aktinischen Keratosen erneut mit Solaraze® behandelt. Nach der zweiten Applikation trat eine akute Dermatitis der Kopfhaut auf.
Weitere zwei Jahre später wurde auch Ciprofloxacin erneut eingenommen, nach zwei Tagen trat ein generalisiertes Exanthem auf.
Befund: Capillitium/Stirn: initial rote Papeln, im Verlauf Vesikel und braun-gelbe Serokrusten auf gerötetem, ödematös geschwollenem Grund ([Abb. 11]).


Diagnostik: Eine allergologische Testung ergab eine dreifach positive Reaktion auf Solaraze-Gel.
Die Testung auf die in Solaraze-Gel enthaltenen Hilfsstoffe Natriumhyaluronat, Polyethylenglykolmonomethylether und Benzylalkohol zeigte sich negativ. Reines Diclofenac lag als Testsubstanz nicht vor.
Kommentar: Solaraze® ist seit 2001 zur Behandlung von aktinischen Keratosen in Deutschland auf dem Markt. Diclofenac hemmt die Cyclooxygennase-2 und somit die Prostaglandin-E-Synthese. Hierdurch soll die Apoptose in Tumorzellen induziert und die Angiogenese gehemmt werden.
Insgesamt wird Solaraze als nebenwirkungsarm eingestuft. Die am häufigsten genannten Nebenwirkungen sind lokale Hautreaktionen, im Sinne einer irritativen Kontaktdermatitis. In der Literatur werden aber auch allergische Kontaktekzeme durch Diclofenac in Solaraze-Gel beschrieben. Zusätzlich wurde über photoallergische Reaktionen berichtet [1 – 3]. Nach Fachinformation sollen Typ-IV-Sensibilisierungen bei 2,18 % der Behandelten vorkommen.
Beschrieben werden auch Sensibilisierungen gegen die Hilfsstoffe in Solaraze. Polyethylenglykolmonomethylether dient zur Lösung von Diclofenac und kann Kontaktallergen sein, ebenso wie der zur Konservierung dienende und in Duftstoffen verwendete Benzylalkohol [3, 4]. Sensibilisierung gegen Hyaluronsäure in Solaraze wurden nach unserem Wissen bisher nicht beschrieben.
Es ist wichtig, die potenziellen Allergene mittels Epikutantest zu identifizieren, da sie zum einen in anderen Grundlagen enthalten sein können und zum anderen kann eine Sensibilisierung gegen Diclofenac bei systemischer Aufnahme zu einer generalisierten Reaktion führen.
In dem beschriebenen Fall stellten wir die Diagnose einer Typ-IV-Allergie gegen Diclofenac. Von einer erneuten lokalen und systemischen Anwendung wurde abgeraten.
Zudem lag eine Ciprofloxacin-Allergie vor, welche sich durch die typische Klinik nach mehrfacher natürlicher Exposition zeigte.
Literatur
1 Kerr OA, Kavanagh G, Horn H. Allergic contact dermatitis from topical diclofenac in Solaraze gel. Contact Dermatitis 2002; 47: 175
2 Kowalzick L, Ziegler H. Photoallergic contact dermatitis from topical diclofenac in Solaraze gel. Contact Dermatitis 2006; 54: 348 – 349
3 Kleyen CE, Bharati A, King CM. Contact dermatitis from 3 different allergens in Solaraze gel. Contact Dermatitis 2004; 51: 215 – 216
4 Taibjee SM, Prais L, Foulds IS. Allergic contact dermatitis from polyethylene glycol monomethyl ether 350 in Solaraze gel. Contact Dermatitis 2003; 49: 170 – 171
Arzneimittelexanthem unter Telaprevir
P. Kleimann
Anamnese: Wir berichten über 2 Patienten mit Exanthemen unter Telaprevir.
Fall 1: Eine 70-jährige Patientin wurde mit stark juckendem und progredientem Exanthem, das sich etwa 2 Wochen nach der ersten Einnahme von Telaprevir im Rahmen einer Kombinationstherapie wegen einer chronischen Hepatitis C entwickelt hatte, aufgenommen. Der Ausschlag hatte am Stamm begonnen und sich im Verlauf über mehrere Wochen hinweg verschlechtert.
Fall 2: Eine 62-jährige Patientin hatte seit etwa 4 Wochen zunehmende juckende Hautveränderungen und seit 8 Wochen Telaprevir aufgrund ihrer chronischen Hepatitis C erhalten.
Untersuchungsbefund: Fall 1: Betont am Stamm findet sich ein stark juckendes makulo-papulöses Exanthem ([Abb. 12]).


Fall 2: Es finden sich konfluierende urtikarielle Makulae an Dekolleté, Armen und Beinen.
Diagnostik: Fall 1: Histologisch zeigte sich ein eosinophilen- und neutrophilenreiches Infiltrat dermal, vereinbar mit einer Arzneireaktion.
Therapie und Verlauf: Fall 1: Telaprevir wurde abgesetzt. Die Patientin erhielt initial einen Steroidstoß, Antihistaminika und topisch Triamcinolon 0,1 % in DAC-Basis-Creme. Zusätzlich wurde eine UVA1-Lichtherapie begonnen. Darunter besserte sich der Hautbefund deutlich. Die antivirale Therapie wurde mit Ribavirin und Peginterferon alfa fortgesetzt.
Fall 2: Es erfolgte eine symptomatische antipruriginöse Therapie mit Tavegil, lokal wurden topische Steroide eingesetzt, des Weiteren erhielt die Patientin eine UVA1-Lichtherapie. Daraufhin besserte sich der Befund langsam, die antivirale Therapie konnte fortgeführt werden.
Kommentar: Telaprevir (Incivo®) gehört zur relativ neuen Substanzklasse der HCV-Proteaseinhibitoren und ist seit 09/2011 zur Therapie der chronischen Hepatitis C bei Erwachsenen in Kombination mit Peginterferon alfa und Ribavirin zugelassen. Auch unter der Zweifach-Therapie mit Peginterferon/Ribavirin treten regelmäßig dermatologische Nebenwirkungen in Form von generalisiertem Pruritus, Xerosis cutis und teilweise Ekzemen auf. Die Hautreaktionen, die während der Tripeltherapie mit Telaprevir beobachtet werden, sind schwerer in ihrer Ausprägung. In den Phase-II- und -III-Studien mit Telaprevir entwickelten etwa die Hälfte der Patienten ein Exanthem durch die Kombinationstherapie. Über 90 % dieser Exantheme waren jedoch mild und konnten mittels topischer Therapie behandelt werden. Ein mildes bis moderates Exanthem erfordert in der Regel keine Beendigung der Tripeltherapie. In einigen Fällen sind jedoch auch schwere Hautreaktionen wie DRESS/HSS oder Stevens-Johnson-Syndrom (SJS) und Toxische epidermale Nekrolyse (TEN) aufgetreten. In diesen Fällen muss die Therapie mit Telaprevir sofort beendet werden. Falls innerhalb von 7 Tagen keine Besserung eintritt, sollten auch die beiden anderen Wirkstoffe der Kombinationstherapie abgesetzt werden. Der Hersteller von Incivo® hat bereits einen „Management-Plan“ für Hautreaktionen unter Telaprevir herausgegeben, der gute Orientierungsmöglichkeiten für die Therapie dieser Nebenwirkung liefert [3].
Literatur
1 Cacoub P, Bourlière M, Lübbe J, Dupin N, Buggisch P, Dusheiko G, Hézode C, Picard O, Pujol R, Segaert S, Thio B, Roujeau JC. Dermatological side effects of hepatitis C and its treatment: Patient management in the era of direct-acting antivirals. J Hepatol 2012; 56: 455 – 463
2 Lawitz EJ. Diagnosis and Management of Telaprevir-Associated Rash. Gastroenterol & Hepatol 2011; 7: 469 – 471
3 http://www.incivekhcp.com/assess-and-manage-rash
Systemische Amyloidose
J. Ter-Nedden
Anamnese: Seit einem Jahr entwickelte der Patient zunehmend rote Flecken perioral. Seit ca. 4 Wochen juckten diese Bereiche verstärkt. Vorstellungen in der HNO und der Hämophilieambulanz waren bis auf eine am ehesten reaktive Faktor-VIII-Erhöhung ohne auffälligen Befund. Es bestand Alkoholabusus. Der Patient befand sich zur Zeit der Vorstellung noch in weiterer Abklärung eines Oropharynx-Karzinoms rechts buccal.
Untersuchungsbefund: Perioral, nasal und vereinzelt am Hals fanden sich Ekchymosen, Hyperpigmentierungen und wachsartige, juckende Plaques ([Abb. 13]). Sonst altersentsprechender Hautbefund.


Diagnostik: AK-Diagnostik: pANCA, cANCA und ANA negativ.
Histologisch fand sich in multiplen Hautbiopsien ein teilweise globuläres eosinophiles Material in der papillären Dermis. Ausgedehnte Hämorrhagien und eine mäßig ausgeprägte Pigmentinkontinenz. Die Eisenfärbung zeigte sich fokal positiv, Kongorot bestätigte den bereits lichtmikroskopischen Befund der Amyloidablagerungen.
Therapie und Verlauf: Vor den geplanten Rektum- und Leberbiopsien verstarb der Patient.
Kommentar: Amyloidosen sind Erkrankungen, deren Entität bis heute nicht vollständig geklärt ist. Das sich in der Haut oder anderen Körperorganen ablagernde Zwischenprodukt der Amyloide besteht aus einer Gruppe heterogener Proteine, welche sich ultrastrukturell ähnlich sind bzw. bei histologischer Anfärbung gleich reagieren. Histologisch zeigen sich bei primär kutanen Amyloidosen in der papillären Dermis Ablagerungen von Amyloid. Dieses lässt sich mittels Kongorot anfärben.
Am plausibelsten erscheint die Erklärung, dass in apoptotischen Keratinozyten die α-Helixstruktur der Keratine in eine ß-Faltblattstruktur umgewandelt wird. Diese Abbauprodukte können von körpereigenen Makrophagen nicht abgebaut werden und verbleiben als Keratinamyloid in der papillären Dermis.
Als alternativer Pathomechanismus wird vorgeschlagen, dass die Expression von Amyloidvorstufen durch monoklonale oder polyklonale Plasmazellen erfolgt.
Klinisch wird zwischen zwei Varianten unterschieden: kutane Amyloidosen mit ursächlichen Keratinamyloidosen wie z. B. Lichen amyloidosus oder makulöse Amyloidose. Ebenfalls in die kutane Variante fällt die AL-Amyloidose. Klinisch entspricht diese der nodulären kutanen Amyloidose. Systemische Amyloidosen (mit unter Umständen auftretenden kutanen Sekundärmanifestationen) können beispielsweise bedingt sein durch lymphoproliferative Prozesse, chronische Entzündungen, hereditäre Erkrankungen oder Langzeitdialyse.
Bei der Therapie muss zwischen der kutanen Variante oder der systemischen Form unterschieden werden:
Kutane Amyloidosen werden in erster Linie mit topischer oder intraläsionaler Kortikosteroid-Applikation behandelt. Auch kann Dimethylsulfoxid (DMSO) topisch oder oral angewendet werden, unter Therapien mit Acitretin oder Cyclophosphamid werden Besserungen berichtet. Systemische Amyloidosen werden durch die Therapie der zugrunde liegenden Erkrankung behandelt.
Literatur
1 Steciuk A, Dompmartin A, Troussard X, Verneuil L, Macro M, Comoz F, Leroy D. Cutaneous amyloidosis and possible association with systemic amyloidosis. Int J Dermatol 2002; 41: 127 – 132
2 Schreml S, Szeimies RM, Landthaler M, Babilas P. Cutaneous amyloidosis. Hautarzt 2011; 62: 55 – 61
Noduläre Amyloidose
C. Gieding
Anamnese: Der 68-jährige Patient stellte sich erstmals im Juli 2012 mit einer seit ca. 4 Jahren bestehenden, symptomlosen, rötlichen Plaque am linken Nasenflügel vor. Er fühlte sich zunehmend ästhetisch gestört und wünschte daher eine Behandlung. Bereits 2009 sei eine noduläre Amyloidose bioptisch gesichert worden. Die bisherigen Behandlungsmaßnahmen (Exzision, Laserbehandlung mittels Erbium-YAG-Laser) waren wegen rascher Rezidive erfolglos. Es bestanden keine weiteren Erkrankungen und keine Hinweise auf eine systemische Amyloidose.
Untersuchungsbefund: Am linken Nasenflügel zeigte sich eine ca. 1×1,5 cm große weiche, rot-bräunliche, reizlose Plaque, am rechten Nasenflügel eine ebenfalls rotbräunliche Plaque ([Abb. 14a]).






Histologischer Befund: In der HE-Färbung fand sich intaktes Epithel mit flacher Hornschicht. Die eosinophil tingierte Basalmembran erschien leicht verbreitert. In der Dermis fand sich diskret entzündliches Infiltrat im Bereich amorphen Materials ([Abb. 14 b]). Die Kongorot-Färbung war positiv ([Abb. 14 c]). Die Bindegewebsstruktur aus elastischen und kollagenen Fasern war aufgehoben.
Diagnostik: Serumelektrophorese und Laboruntersuchungen (GOT/GPT/GGT/Bili/Krea/Elektrolyte) waren ohne pathologischen Befund.
Diagnose: Noduläre Amyloidose.
Therapie: Eine topische Therapie mit Mometasonfuroat-Fettcreme zeigte keine Wirkung. Deshalb wurde mit einem Diodenlaser (940 nm, aufsteigende Dosierungen, zuletzt 376 J/cm2, 1,5 mm) behandelt. Nach 5 Behandlungen waren die Knoten deutlich abgeflacht.
Kommentar: Die noduläre Amyloidose ist eine seltene Form der primär kutanen Amyloidose. Die Ätiologie ist unklar. Typischerweise treten Papeln und Plaques am Stamm, den Extremitäten, in der Genitalregion oder im Gesicht auf. Tendenziell werden die Akren bevorzugt. Zur Therapie wurden folgende Verfahren eingesetzt: topische Kortikosteroide der Klasse III und IV (auch okklusiv), intraläsionale Injektion von Triamcinolon, Exzision lokalisierter Befunde, Shave-Exzision, Kürettage oder Dermabrasion. In den meisten Fällen muss hier jedoch mit einem Rezidiv gerechnet werden. Nach Vaporisierung mittels CO2 sollen die Behandlungerfolge länger anhalten [1]. Fallberichte über den Einsatz eines Erbium-Yag-Lasers existieren bisher nur für den Lichen amyloidosus im fraktionierten Modus mit ebenfalls guten Ergebnissen. Ein Patient wurde erfolgreich mit einem Farbstofflaser (585 nm) behandelt [2]. Bei unserem Patienten entschieden wir uns aufgrund der vorangegangenen Rezidive und der Dicke der Plaques für einen Therapieversuch mit Diodenlaser. Ähnlich wie beim Farbstofflaser könnte hier die mikrovaskuläre Durchblutung verringert werden oder man koaguliert die abgelagerten Amyloide. Nach mehrfacher Wiederholung der Behandlung (Abstände 6 – 8 Wochen) waren die Plaques deutlich abgeflacht.
Literatur
1 Truhan AP, Garden JM, Roenigk HH Jr. Nodular primary localized cutaneous amyloidosis: immunohistochemical evaluation and treatment with the carbon dioxide laser. J Am Acad Dermatol 1986; 14: 1058 – 1062
2 Alster TS, Manaloto RM. Nodular amyloidosis treated with a pulsed dye laser. Dermatol Surg 1999; 25: 133 – 135
Korymbiformes Syphilid (Bombensyphilid)
L. Meister
Anamnese: Die Patientin bemerkte erstmals vor fünf Monaten kleine symptomlose Papeln an der linken Brust, die sich im Verlauf zentrifugal ausbreiteten. Ansonsten war die Patientin gesund. Eine Vorbehandlung erfolgte bisher nicht.
Untersuchungsbefund: Es fand sich links pektoral eine erythematöse Plaque umrandet von gruppiert stehenden, teilweise konfluierenden, rotbräunlichen, derben, bis erbsgroßen Papeln ([Abb. 15 a]).
Diagnostik: Histologisch zeigte sich ein granulomatöses Entzündungsinfiltrat mit Nachweis von Riesenzellen, begleitet von einer lymphohistiozytären Entzündungsreaktion mit einzelnen plasmazytoiden Zellen ([Abb. 15 b], histologisches Präparat mit freundlicher Unterstützung der Praxis Dres. med. Becker/Mayet, Frankfurt).




Molekularpathologisch gelang der Nachweis von Treponema pallidum. TP-PA-positiv, VDRL 1 : 16, Antikörper gegen Treponema pallidum IgM- und IgG-positv. HIV-Test negativ.
Eine neurologische Beteiligung konnte mittels Liquordiagnostik und Aortengummen mittels Röntgen Thorax ausgeschlossen werden.
Therapie und Verlauf: Unter der Diagnose eines korymbiformen Syphilids (Bombensyphilid) erhielt die Patientin dreimalig Benzylpenicillin (Tardocillin) 2,4 Mega i. m. im wöchentlichen Abstand. Um eine Jarisch-Herxheimer-Reaktion zu verhindern, nahm sie initial 30 Minuten vor der i. m.-Injektion 40 mg Urbason ein. Drei Monate später zeigte sich links pektoral lediglich noch eine postinflammatorische Hyperpigmentierung. Weitere klinische und serologische Kontrollen sind nach 3, 6 und 12 Monaten geplant.
Kommentar: Das korymbiforme Syphilid ist eine Läsion der frühen sekundären Lues ohne bevorzugte Lokalisation mit korymbiform (blütentraubenartig) angeordneten Papeln aus typischerweise zentral größeren und peripher zerstreuten, kleineren Papeln. Histologisch stellt sich eine granulomatöses Infiltrat dar, sodass die Differenzialdiagnose zu anderen granulomatösen Erkrankungen schwierig ist.
Anamnestisch ließ sich der Infektionszeitpunkt der Patientin nicht mehr zuordnen.
Die Therapie der Wahl ist Penicillin intramuskulär als Bolus. Bei Penicillinallergie kann Doxycyclin, Erythromycin oder Azithromycin oral gegeben werden.
Literatur
1 Angus J, Langan SM, Stanway A, Leach IH, Littlewood SM, English JS. The many faces of secondary syphilis: a re-emergence of an old disease. Clin Exp Dermatol 2006; 31: 741 – 745
2 Baughn RE, Musher DM. Secondary syphilitic lesions. Clin Microbiol Rev 2005; 18: 205 – 216
3 Schrader AM, Rácz E, Noordhoek Hegt V, van der Snoek EM, van Praag MC. [Granulomatous secondary syphilis; an uncommon presentation of a polymorphic disease.] Ned Tijdschr Geneeskd 2012; 155: A5130
Hautveränderungen bei primärer Immundefizienz
A. Messerschmidt
Anamnese: Bei dem zehn Wochen alten Patienten besteht seit der Geburt eine sehr trockene Haut. Im Alter von zwei Wochen wurde er wegen eines generalisierten Exanthems unter dem Verdacht auf eine Virusinfektion in einer anderen Klinik stationär symptomatisch behandelt. Nach Entlassung entwickelte sich ein fettig-schuppendes Hautbild, welches als seborrhoisches Ekzem interpretiert wurde ([Abb. 16]). Im Alter von vier Wochen wurde der Patient erstmals in unserer Klinik unter dem Verdacht auf ein atopisches Ekzem stationär behandelt. Unter einer topischen Kortikoidtherapie und Applikation antiseptischer und antimykotischer Externa besserte sich der Befund, verschlechterte sich aber sofort wieder nach dem Absetzen der Topika und die Ohren begannen zusätzlich zu nässen.


Untersuchungsbefund: Im Windelbereich zeigten sich nässende Erosionen, an den Händen schuppende Erytheme mit vereinzelten Pusteln. Außerdem sah man im Gesicht, am Nacken und den Extremitäten Ekzeme ([Abb. 16]).
Diagnostik: Das Blutbild zeigte eine Lymphopenie. Im Pustel- und Rachenabstrich wurden Staphylococcus aureus und Klebsiella oxytocea nachgewiesen.
Therapie und Verlauf: Eine Antibiose mit Cefaclor-Saft wurde initiiert. Topisch erfolgte die Applikation steroidhaltiger und antiseptischer Topika, im Windelbereich von antimykotischen Pasten. Die entzündlichen Erscheinungen waren äußerst therapierefraktär und der Patient entwickelte zusätzlich grünliche Durchfälle, Atembeschwerden und eine ausgeprägte Otorrhoe. Ein Konsil bei den Kollegen der Pädiatrie bestätigte den Verdacht auf das Vorliegen eines Immundefekts und ergab eine „severe combined immunodeficiency disease“ (Prof. Bader, Klinik für Kinder- und Jugendmedizin, Universitätsklinikum Frankfurt).
Kommentar: Primäre Immundefekte umfassen eine Reihe ernsthafter und seltener Erkrankungen hauptsächlich bei Kindern. Ursächlich sind Mutationen in einem oder mehreren Genen, die für eine Komponente des Immunsystems kodieren [1]. Insgesamt leiden etwa 40 – 70 % der betroffenen Patienten unter kutanen Manifestationen [2]. Oftmals sind Hautveränderungen wie Infektionen, Ekzeme und Erythrodermien die ersten Symptome. Dabei sind atypische Präsentationen bekannter Dermatosen häufig. Daher sind dermatohistologische, bakterielle, virale und mykologische Untersuchungen meist unabdingbar. Eine frühzeitige Diagnosestellung kann eine rasche, potenziell lebensrettende Therapieeinleitung ermöglichen. Der vorgestellte Patient erhielt eine Knochenmarktransplantation.
Literatur
1 Sillevis Smitt JH, Wulffraat NM, Kuijpers TW. The skin in primary immunodeficieny disorders. Eur J Dermatol 2005; 15: 425 – 432
2 Lehman H. Skin Manifestations of Primary Immune Deficiency. Clinic Rev Allerg Immunol 2013 (im Druck)
Danksagung
Den Firmen Abbott Immunology, Almirall Hermal, Bauerfeind, Biogen Idec, GlaxoSmithKline, Janssen-Cilag, Leo Pharma, L’Oréal, Novartis Pharma, Pierre Fabre, Roche Pharma und Stallergenes danken wir für ihre Unterstützung unserer Tagung.
Interessenkonflikt
Die Autoren geben an, dass kein Interessenkonflikt besteht.
Korrespondenzadresse


















































